 Распечатать эту запись
Распечатать эту запись
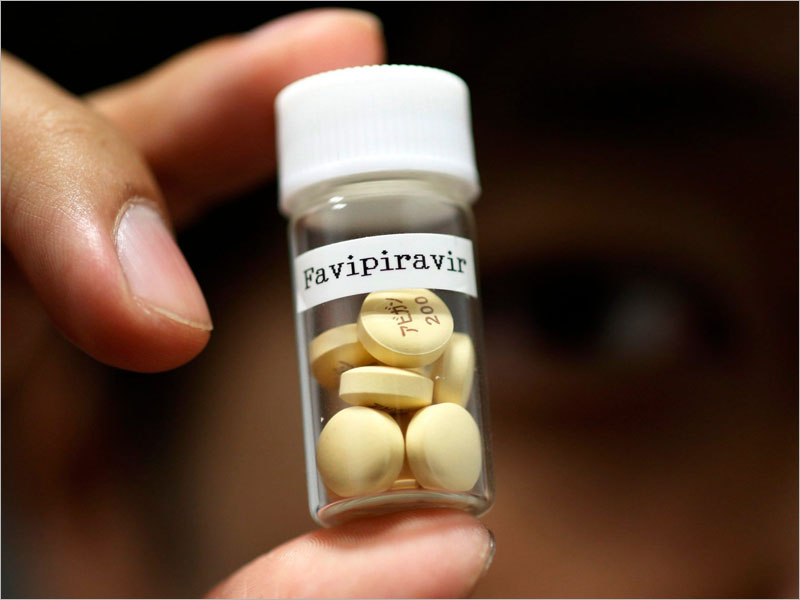
Российский фонд прямых инвестиций (РФПИ) и группа компаний «ХимРар» запустили клинические исследования препарата «Фавипиравир» у пациентов, госпитализированных с COVID-19. Исследования будут проходить в 17 центрах по всей России с участием 330 больных с подтвержденной коронавирусной инфекцией. Первыми начали получать терапию пациенты в трёх медицинских центрах в Москве, Нижнем Новгороде и Смоленске, сообщает пресс-служба РФПИ.
В рамках клинического исследования будет изучена эффективность и безопасность препарата «Фавипиравир», а также выбран оптимальный режим дозирования пациентов.
Недавно завершившийся первый этап доклинических исследований показал, что «Фавипиравир» можно отнести к пятой (высшей) категории безопасности согласно классификации в Глобальной Гармонизированной Системе (GHS). Препарат продемонстрировал противовирусную активность in vitro и продолжает изучатся in vivo на моделях вируса SARS-COV-2 (штамм nCoV/Victoria/1/2020). Доклинические исследования продолжаются совместно с ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи» и ФБУН ГНЦ ВБ «Вектор» Роспотребнадзора России.
В экспресс-исследовании фармакокинетики животных «Фавипиравир» показал высокую биодоступность при пероральном приёме, что согласуется с литературными данными — на лабораторных животных биодоступность составила более 75%.
В настоящее время «ХимРар» активно ведет наработку субстанции и производство готовой лекарственной формы препарата. После получения государственного одобрения, «ХимРар» приступит к выпуску препарата на рынок, при этом, значительная часть пациентов с коронавирусом сможет получить его в рамках клинических исследований уже в первой декаде мая. #bryakingnews
Обсуждение ( 0 комментариев )